|
|

|
| ||
|
|
||
► Боби I. Аминҳо. Аминокислотаҳо. Пайвастагиҳои ҳетеросиклии нитрогендор
► Амидҳо:сохт, истеҳсол ва хосиятҳои онҳо
► Аминокислотаҳо
► Намунаҳои ҳалли мисол ва масъалаҳо
► Мисол ва масъалаҳо барои ҳалли мустақилона
► Пайвастагиҳои ҳетеросиклии нитрогендор
► Савол ва супоришҳо ва таҷрибаҳои лабораторӣ
► Боби IV. Синтези моддаҳои калонмолекула ва масолеҳи полимерӣ дар асоси онҳо
► Методҳои асосии синтези полимерҳо
► Полимеризатсия
► Моддаҳои пластикӣ
► Каучукҳои синтезӣ
► Нахҳои синтезӣ
► Саволҳо ва таҷрибаҳои лабораторӣ ► Мисол ва масъалаҳо барои ҳалли мустақилона
► Боби V. Ҷамъбасти омӯзиши курси химияи органикӣ
► Намудҳои изомерия
► Изомерияи структурӣ
► Изомерияи занҷири атомҳои карбон
► Изомерияи ҳолати бандҳои дучанда ва сечанда дар молекула
► Изомерияи ҳолати гурӯҳҳои функсионалӣ ё атомҳои алоҳида дар молекула
► Изомерияе, ки ба пайвастагиҳои органикии дар таркиби молекулаашон ҳалқаи бензолӣ дошта хос аст
► Изомерияи фазоӣ ё стереоизомерия
► Табиати электронии банди химиявӣ
► Синтезҳои муҳими саноатӣ дар асоси коркарди нафт ва дигар ашёҳои карбоҳидрогенӣ
► Намунаи ҳалли масъалаҳо ва саволҳо барои ҷавоб
► Масъалаҳо барои ҳалли мустақилона
► Системаи даврии муосири элементҳои химиявӣ
► Мавқеи лантаноидҳо ва актиноидҳо дар системаи даврии элементҳои химиявӣ
► Валентнокӣ ва имкониятҳои валентии атомҳо
► Саволҳо барои ҷавоб ва намунаи ҳалли масъалаҳо
► Масъалаҳо барои ҳалли мустақилона
► Сохти фазоии молекулаи моддаҳои органикӣ ва ғайриорганикӣ
► Навъҳои панҷараҳои кристаллӣ ва хосияти моддаҳо
► Пайвастагиҳои комплексӣ
► Ададҳои координатсионӣ
► Системаҳои дисперсӣ
► Саволҳо барои ҷавоб ва намунаҳои ҳалли масъалаҳо
► Масъалаҳо барои ҳалли мустақилона
► Боби VIII. Реаксияҳои химиявӣ
► Таснифи реаксияҳои химиявӣ
► Суръати реаксияҳои химиявӣ
► Қонуни таъсири масса. Собити мувозинат
► Принсипи Ле-Шателе. Лағжиши мувозинати химиявӣ
► Катализ ва гидролиз
► Саволҳо барои ҷавоб ва намунаҳои ҳалли масъалаҳо
► Масъалаҳо барои ҳалли мустақилона
► Саҳми олимони асрҳои миёнаи тоҷик дар инкишофи химия
► Асосҳои илмӣ ва принсипҳои умумии технологияи химиявӣ
► Химия ва ҳифзи муҳити зист
► Химия дар ҳаёти мо
► Химиконии кишоварзӣ
► Саволҳо барои ҷавоб
► Замима
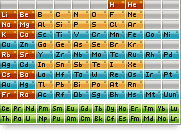

СИСТЕМАИ ДАВРИИ МУОСИРИ ЭЛЕМЕНТҲОИ ХИМИЯВӢ
Системаи даврии элементҳои химиявӣ танҳо дар асоси механикаи квантӣ
шарҳи ҳудро ёфт. Шакли кӯтоҳи системаи даврии элементҳо, ки
Д.И.Менделеев ба он таваҷҷӯҳ дошт, сохти электронӣ ва хосияти химиявии
элементҳоро пурра таҷассум карда наметавонад. Аз ин сабаб аз тарафи
ИЮПАК шакли дарози системаи даврии элементҳои химиявӣ пешниҳод карда шуд,
ки сохти электронӣ ва хосиятҳои химиявии элементҳоро пурратар инъикос
менамояд.
Шакли дарози системаи даврии элементҳо, ки онро минбаъд
системаи даврии муосири элементҳо ё системаи даврии элементҳо мегӯем,
дар саҳифаҳои 96-97 оварда шудааст.
Системаи даврии муосир, нисбат ба шакли қӯтоҳи системаи
даврӣ соддатар аст. Системаи даврӣ аз 7 давр ва 18 гурӯҳ иборат аст. Ҳар
давр аз як қатор иборат буда, ҳамон элементҳоеро дар бар мегирад, ки
рақами қабати болотарини электрониашон ба рақами ҳамин давр баробар
бошад.
Масалан, ҳелий дар даври 1-ум, калий дар даври 4-ум, нуқра
дар даври 5-ум ҷойгир шудаанд. Дар ҳар гурӯҳ элементҳое ҷойгиранд, ки
новобаста ба қабати болотарини электронӣ, дар қишри болотарини
электрониашон миқдори якхелаи электронҳо доранд. Масалан, дар гурӯҳи
1-ум элементҳое ҷойгир шудаанд, ки дар қишри болотаринашон (қишри s) як
электрон доранд: Н, Li, Na, К, Rb, Cs ва Fr.
Шумо медонед, ки миқдори электронҳо дар элемент ба рақами
тартибии ин элемент дар системаи даврӣ баробар аст. Миқдори электронҳои
элементро дониста дар асоси таълимоти механикаи квантӣ ҷойгиршавии
электронҳои онро дар қабату қишрҳои электронӣ ёфтан мумкин аст.
Расми 5. Конфигуратсияи электронии атомҳои ҳидроген ва ҳелий
Азбаски
дар қабати якуми электронӣ ду савияи энергӣ мавҷуд аст, дар ин қабат, чӣ
хеле дар боло нишон дода будем, танҳо ду электрон ҷойгир шуда метавонанд.
Ин қабат аз як s қишр иборат аст. Электронҳое, ки дар ин қишр ҷойгиранд,
s электронҳо ном доранд. Даври якум танҳо ду элемент дорад: ҳидроген ва
ҳелий. Конфигуратсияҳои электронии ин элементҳо дар расми 5 нишон дода
шудаанд.
Элементҳои даври дуюм ду қабати электронӣ доранд. Азбаски дар
қабати дуюм танҳо 8 савияи энергӣ мавчуд аст, даври дуюм аз 8 элемент
иборат аст. Литий (Li) се электрон дорад, 2 электрон дар қабати якум
ҷойгир шуда, электрони сеюм дар S қишри қабати дуюм ҷойгир мешавад.
Конфигуратсияи электронии он чунин аст: 1S22S1.
Дар элементи бериллий (Be) электронҳояш S қишрҳои ҳар ду қабатро ишғол
менамоянд ва аз ин сабаб конфигуратсияи электронии он 1S22S2
мебошад.Аз бор (В)
сар карда, пуршавии р-қишри
қабати дуюм оғоз ёфта дар элементи неон (Ne) ба охир мерасад.
Электронҳое, ки дар р-қишр ҷойгиранд р-электронҳо номида мешаванд.
Конфигуратсияи электронии неон (Ne) чунин аст: 1s22s22p6.
Ба таври графикӣ ҷойгиршавии электронҳои неонро дар
қабату қишрҳои электронӣ чунин ифода мекунанд:
Дар қабати
сеюми электронӣ 18 савияи энергӣ мавҷуд аст, вале дар даври сеюми
системаи даврӣ ҳамагӣ 8 элемент ҷойгир шудаанд. Сабаби ин дар он аст, ки
аз натрий (Na) cap карда то аргон (Ar) қабати сеюми электронӣ бо як
низоми муаӣян то d-қишр пур карда мешавад. Аз ин сабаб навиштани
конфигуратсияи электронии элементҳои даври сеюми системаи даврӣ он қадар
душвор нест. Масалан, конфигуратсияи электронии натрий (Ха) 1s22s22p63s1,
фосфор (P) 1s22s22p63s23p3
ва аргон (Ar) 1s22s22p63s23p6
мебошад. Аз калий (K) пуршавии d-қишри қабати
сеюм бояд сар мешуд. Вале бо сабаби он, ки савияҳои энергии
s-қишри қабати чорум нисбат ба савияҳои
энергии d-қишри қабати сеюм поёнтар ҷойгир
шудаанд, бинобар ин, аввал, савияҳои энергии s-қишри
қабати чорум пур шуда, сипас d-қишри қабати
сеюм пур карда мешавад.
Аз ин сабаб даври чоруми системаи даврӣ аз элементи
калий (K) cap мешавад. Дар атоми калий (K) электрони нуздаҳум дар
s-қишри қабати чорум ҷойгир мешавад, вале d-қишри
қабати сеюм холӣ мемонад. Конфигуратсияи электронии он чунин аст:
Дар бисёр мавридҳо ҷойгиршавии электронҳоро дар қабату қишрҳо ба шакли кӯтоҳ нишон медиҳанд:
Дар элементи калсий (Са) (рақами тартибиаш 20) электрони бистум, s-қишри қабати чорумро пур мекунад. Конфигуратсияи электронии он чунин аст:
Аз элементи скандий (Sc) (рақами тартибиаш 21) cap карда, бо дар назардошти он, ки s-қишри қабати чорум пур аст, пуршавии d-қишри қабати сеюм cap мешавад. Азбаски дар d-қишр 10 савияи энергӣ мавҷуд аст, аз элементи скандий (Sc) cap карда, то элементи руҳ (Zn) d-қишри қабати сеюм пур мегардад. Электронҳое, ки дар d-қишр ҷойгиранд, d-электронҳо номида мешаванд. Конфигуратсияи электронии скандий (Sc) чунин аст:
Ҷойгиршавии электронҳои элементи скандий (Sc) дар қабатҳои электронӣ шакли зеринро дорад:
Конфигуратсияи электронии руҳ (Zn) чунин аст:
Ҷойгиршавии электронҳои руҳ Zn дар қабатҳои электронӣ бошад, намуди зеринро дорад:
Пуршавии d-қишри қабати сеюм барои элементҳои хром (Cr) ва мис (Cu) ғайричашмдошт аст. Мутобиқи пуршавии дар боло овардашуда конфигуратсияи электронии хром (Cr) бояд чунин бошад:
Вале дар асл яке аз электронҳои s-қишри қабати чоруми электронӣ ба d-қишри қабати сеюм мегузарад. Аз ин сабаб конфигуратсияи воқеии хром (Cr) чунин аст:
Ин гуна гузариш, ки «афтиши» электрон ном дорад, дар мис (Cu) низ
мушоҳида мешавад.
Аз галлий (Ga) cap карда
пуршавии р-қишри қабати чорум оғоз
ёфта, дар элементи криптон (Kr) ба анҷом мерасад. Конфигуратсияи
электронии элементи криптон (Kr) чунин аст:
Даври чоруми системаи даврӣ бо криптон (Kr) ба анҷом мерасад ва
аз 18 элемент иборат аст.
Даври 5-уми
системаи элементҳо аз элементи рубидий (Rb) оғоз
меёбад. Электрони сию ҳафтуми рубидий Rb дар s-қишри
қабати панҷум ҷойгир мешавад, ҳол он, ки d ва f-қишрҳои
қабати чорум ҳануз холианд. Дар элементи стронсий (Sr) электрони навбатӣ
(сию ҳаштум) дар s-қишри қабати панҷум ҷойгир
мешавад.
Аз элементи итрий (Y)
(рақами тартибиаш 39) то элементи қадмий (Cd)
(рақами тартибиаш 48) d-қишри қабати чорум бо
электронҳо пур карда мешавад.
Аз элементи индий (In) (рақами
тартибиаш 49) то элементи ксенон (Хе) (рақами тартибиаш 54) электронҳои
навбатӣ дар р-қишри қабати панҷум ҷойгир
мешаванд. Конфигуратсияи электронии ксенон (Хе) чунин аст:
Ҷойгиршавии электронҳои ксенон (Хе) дар кабатҳои электронӣ шакли зеринро дорад:
Ҳамин тавр, даври панҷуми
системаи даврӣ 18 элемент дорад ва дар онҳо f-қишри
қабати чорум холӣ аст.
Даври шашуми системаи
даврӣ бо элементҳои сезий (Cs) ва барий (Ва) оғоз
меёбад, ки электронҳои панҷоҳу панҷум ва панҷоҳу
шашуми онҳо дар s-қишри қабати шашум
ҷойгир мешаванд.
Дар атоми лантан (La) (рақами тартибиаш 57) электрони панҷоҳу ҳафтум дар
d-қишри қабати чорум ҷойгир мешавад.
Аз элементи серий
(Се) (рақами тартибиаш 58) cap карда то элементи лютетсий (Lu) (рақами
тартибиаш 71) электронҳо f-қишри қабати
чорумро пур мекунанд. Дар системаи даврӣ аз серий cap карда то лютетсий
14 элемент ҷой гирифтаанд. Ин гурӯҳи элементҳоро лантаноидҳо меноманд.
Аз сабаби он, ки дар ин элементҳо қабату қишри электронии болотаринашон
якранг аст, онҳо хосияти химиявии монанд зоҳир мекунанд.
Аз гафний (Hf) (рақами
тартибиаш 80) cap карда пуркунии d-қишри
қабати панҷум идома меёбад. Аз элементи талий (Tl) (рақами тартиби аш
81) то радон (Rn) (рақами тартибиаш 86) электронҳо 6р-қишрро
пур мекунанд. Даври шашум бо элементи (Rn) ба охир мерасад. Ин давр сию
ду элемент дорад.
Пуршавии даври ҳафтум,
ки ҳануз нотамом аст, ба пуршавии даври шашум монанд аст.