|
|

|
| ||
|
|
||
► Боби I. Аминҳо. Аминокислотаҳо. Пайвастагиҳои ҳетеросиклии нитрогендор
► Амидҳо:сохт, истеҳсол ва хосиятҳои онҳо
► Аминокислотаҳо
► Намунаҳои ҳалли мисол ва масъалаҳо
► Мисол ва масъалаҳо барои ҳалли мустақилона
► Пайвастагиҳои ҳетеросиклии нитрогендор
► Савол ва супоришҳо ва таҷрибаҳои лабораторӣ
► Боби IV. Синтези моддаҳои калонмолекула ва масолеҳи полимерӣ дар асоси онҳо
► Методҳои асосии синтези полимерҳо
► Полимеризатсия
► Моддаҳои пластикӣ
► Каучукҳои синтезӣ
► Нахҳои синтезӣ
► Саволҳо ва таҷрибаҳои лабораторӣ ► Мисол ва масъалаҳо барои ҳалли мустақилона
► Боби V. Ҷамъбасти омӯзиши курси химияи органикӣ
► Намудҳои изомерия
► ӣзомерияи структурӣ
► ӣзомерияи занҷири атомҳои карбон
► ӣзомерияи ҳолати бандҳои дучанда ва сечанда дар молекула
► ӣзомерияи ҳолати гурӯҳҳои функсионалӣ ё атомҳои алоҳида дар молекула
► ӣзомерияе, ки ба пайвастагиҳои органикии дар таркиби молекулаашон ҳалқаи бензолӣ дошта хос аст
► ӣзомерияи фазоӣ ё стереоизомерия
► Табиати электронии банди химиявӣ
► Синтезҳои муҳими саноатӣ дар асоси коркарди нафт ва дигар ашёҳои карбоҳидрогенӣ
► Намунаи ҳалли масъалаҳо ва саволҳо барои ҷавоб
► Масъалаҳо барои ҳалли мустақилона
► Системаи даврии муосири элементҳои химиявӣ
► Мавқеи лантаноидҳо ва актиноидҳо дар системаи даврии элементҳои химиявӣ
► Валентнокӣ ва имкониятҳои валентии атомҳо
► Саволҳо барои ҷавоб ва намунаи ҳалли масъалаҳо
► Масъалаҳо барои ҳалли мустақилона
► Сохти фазоии молекулаи моддаҳои органикӣ ва ғайриорганикӣ
► Навъҳои панҷараҳои кристаллӣ ва хосияти моддаҳо
► Пайвастагиҳои комплексӣ
► Ададҳои координатсионӣ
► Системаҳои дисперсӣ
► Саволҳо барои ҷавоб ва намунаҳои ҳалли масъалаҳо
► Масъалаҳо барои ҳалли мустақилона
► Боби VIII. Реаксияҳои химиявӣ
► Таснифи реаксияҳои химиявӣ
► Суръати реаксияҳои химиявӣ
► Қонуни таъсири масса. Собити мувозинат
► Принсипи Ле-Шателе. Лағжиши мувозинати химиявӣ
► Катализ ва гидролиз
► Саволҳо барои ҷавоб ва намунаҳои ҳалли масъалаҳо
► Масъалаҳо барои ҳалли мустақилона
► Саҳми олимони асрҳои миёнаи тоҷик дар инкишофи химия
► Асосҳои илмӣ ва принсипҳои умумии технологияи химиявӣ
► Химия ва ҳифзи муҳити зист
► Химия дар ҳаёти мо
► Химиконии кишоварзӣ
► Саволҳо барои ҷавоб
► Замима
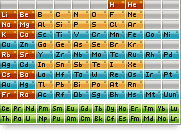

d-МЕТАЛЛҲО
Дар қабати берунаи электронии d-металлҳо, асосан, ду электрон дар s-қишр
мавҷуд буда, d-қишри қабати пешинаи электрони онҳо пай дар пай пур карда
мешавад. Вале дар баъзе элементҳо ҳодисаи «афтиши» электрон мушоҳида
мегардад. Ин ҳодиса аз он иборат аст, ки яке аз
электронҳо аз s-қишри қабати беруна ба d-қишри қабати дохилӣ мегузарад
ва дар натиҷа дар s-қишри қабати беруна як электрон боқӣ мемонад.
Фаъолияти химиявии d-металлҳо дар ҳар як гурӯҳ аз
боло ба поён кам мешавад: Fe-Ru-Os, Co-Ir-Mt, Ni-Pd-Pt, Cu-Ag-Au, Zn-Cd-Hg
ва ғайра.
Ҳамаи d-металлҳо, ба истиснои Zn, якчанд дараҷаи
оксидшавӣ доранд ва хосиятҳои металлиашон нисбат ба хосиятҳои
ғайриметаллиашон бартарӣ дорад. Руҳ танҳо дараҷаи оксидшавии +2 зоҳир
менамояд. Вай намояндаи хоси металлҳои амфотерӣ мебошад.
Дар байни d-металлҳо мис, оҳан, руҳ, титан ва
хром аҳамияти калони истеҳсолӣ доранд ва аз ин сабаб хосиятҳои химиявии
онҳоро пурратар дида мебароем.
d-Металлҳои гурӯҳи 4-уми системаи
даврӣ. Ба ин гурӯҳи системаи даврӣ элементҳои титан, сирконий,
гафний ва резерфордий мансубанд. Атомҳои ин элементҳо дар қабати берунаи
электрониашон ду электрон дар s-қишр дошта, дар қабати поёнтар аз қабати
берунаи электронӣ даҳ электрон доранд, ки аз онҳо ду электрон дар d-қишр
ҷойгиранд. Аз ҳамин сабаб барои ин металлҳо дараҷаи оксидшавии аз ҳама
хос +2 ва +4 буда, дараҷаи оксидшавии +3 кам вомехӯрад.
Титан Ti. Конфигуратсияи ду қабати
оҳирини электронии титан 3s23p63d24s2
мебошад.
Титан аз сабаби бо пардаи оксидӣ пӯшида буданаш, нисбат ба
пӯлоди зангназананда дида ба коррозия устувортар аст.
Дар ҳарорати баланд титан бо ҳалогенҳо, оксиген, сулфур, нитроген
ва дигар элементҳо пайвастагӣ ҳосил мекунад:
Титан бо кислотаи сулфат таъсири мутақобил мекунад ва маҳсули реаксия аз консентратсияи кислота ва ҳарорати реаксия вобаста аст:
Сирконий
Zr. Конфигуратсияи ду қабати охирини электронии сирко ний 4s24p64d25s2
мебошад. Сирконий, чун титан, нисбати коррозия устувории ниҳоят баланд
зоҳир менамояд ва дар ишқорҳо, кислотаҳои сулфат ва хлорид ҳал намешавад.
Дар ҳарорати баланд сирконий бо ҳалогенҳо, оксиген ва нитроген
таъсири мутақобил намуда, оксидҳо, ҳалогенидҳо ва нитриди мувофиқ ҳосил
мекунад. Сирконий дар пайвастагиҳояш бо нитроген дараҷаи оксидшавии +3
ва дар пайвастагиҳояш бо оксиген ва ҳалогенҳо дараҷаи оксидшавии +4
зоҳир менамояд:
d-Металлҳои гурӯҳи 6-уми системаи даврӣ.
Ба ин гурӯҳ металлҳои хром, молибден, волфрам ва сиборгий дохил мешаванд.
Онҳо, ба истиснои хром, дар қабати берунаи электронӣ ду электрон дар s-қишр
дошта, дар қабати поёнтар аз қабати берунаи электронӣ дувоздаҳ электрон
доранд, ки аз ин электронҳо чортояш дар d-қишр ҷойгиранд. Хром дар
қабати берунаи электрониаш як электрон дар s-қишр
дошта, дар қабати поёнтар аз қабати берунаи электрониаш сенздаҳ электрон
дорад, ки аз ин электронҳо панҷтояш дар d-қишр ҷойгиранд. Дараҷаи олии
оксидшавии элементҳои ин гурӯҳ +6 мебошад.
Хром Cr. Конфигуратсияи
ду қабати охирини электронии хром 3s23p64d54s1
мебошад. Хром металли ҷилодори сахт аст. Вай аз сабаби бо пардаи оксидӣ
пӯшида буданаш, ба таъсири ҳаво ва об устувор аст.
Кислотаҳои сулфат ва хлориди
консентратсияашон паст бо хром таъсири мутақобил менамоянд. Ин реаксияҳо
бо хориҷ шудани ҳидроген мегузаранд:
Кислотаи
консентронидаи нитрат пардаи оксидии хромро мустаҳкам менамояд. Аз ин
сабаб хром дар он ҳал намешавад ва пас аз коркарди хром бо кислотаи
консентронидаи нитрат вай нофаъол мегардад.
Хром дар пайвастагиҳояш дараҷаи оксидшавии +2, +3 ва +6 зоҳир
менамояд. Оксиди хром (II) хосияти асосӣ, оксиди хром (III) хосияти
амфотерӣ ва оксиди хром (VI) хосияти кислотагӣ доранд:
Ҳамаи пайвастагиҳои хром (VI) оксидкунандаҳои қавӣ мебошанд:
Молибден Mo. Конфигуратсияи ду қабати охирини электронии молибден 4s24p64d55s1
мебошад. Молибден металли нуқраранг аст.
Дар ҳарорати муқаррарӣ бо оксигени ҳаво таъсири
мутақобил намекунад, вале ҳангоми гарм кардан бо оксиген ба реаксия
дохил шуда оксиди молибден (VI) ҳосил мекунад:
Кислотаҳои хлорид ва сулфати консентратсияашон паст дар ҳарорати
мӯътадил ба молибден таъсир намекунанд. Молибден бо кислотаи нитрат ва
кислотаи консентронидаи сулфати тафсон таъсири мутақобил мекунад.
Барои молибден дараҷаи оксидшавии +6 хос
мебошад, вале пайвастагиҳое низ маълуманд, ки дар онҳо молибден дараҷаи
оксидшавии +2, +3, +4 ва +5 зоҳир менамояд.
Волфрам W. Конфигуратсияи ду қабати
охирини электронии волф рам 5s25p65d46s2
мебошад. Волфрам металли сафеди вазнин аст.
Волфрам нисбат ба таъсири ҳаво, об, кислотаҳо ва ҳатто
шароби шоҳ устувор аст. Вай танҳо дар омехтаи кислотаҳои нитрат ва
фторид ҳал мешавад. Хосиятҳои химиявии волфрам ба хосиятҳои химиявии
молибден монанд аст.
d-Металлҳои гурӯҳи 8-уми системаи даврӣ.
Металлҳои ин гурӯҳ оҳан, рутений, осмий ва хассий мебошанд. Аз сабаби он,
ки дар байни онҳо оҳан аҳамияти бузурги истеҳсолӣ дорад, бинобар ин
хосиятҳои химиявии онро пурратар меомӯзем.
Оҳан Fe. Конфигуратсияи ду қабати охирини
электронии оҳан 3s23p63d64s2
мебошад. Оҳан металли сафеди нуқраранг аст. Вай дорои хосиятҳои магнитӣ
мебошад. Оҳан дар пайвастагиҳояш дараҷаҳои оксидшавии +2 ва +3 зоҳир
менамояд, вале пайвастагиҳое низ маълуманд, ки дар онҳо оҳан дараҷаи
оксидшавии + 1, +4 ва +6 дорад.
Оҳан металли фаъолияташ миёна буда, бо бисёр
ғайриметаллҳо таъсир мекунад:
Дар об оҳан занг мезанад. Агар дар дохили об ба оҳан оксиген дастрас бошад, он гоҳ ҳидроксиди оҳан ҳосил мешавад:
Дар ҳарорати баланд оҳан бо об ба реаксия дохил шуда, ҳидрогенро хориҷ менамояд:
Оҳан бо кислотаи хлорид ҳама вақт бо хориҷ намудани ҳидроген таъсири мутақобил мекунад:
Ҳамин тарз оҳан бо кислотаи сулфати консентратсияаш паст таъсири мутақобил мекунад:
Оҳан бо кислотаи консентронидаи сулфат бо хориҷ намудани SO2 ба реаксия дохил мешавад:
Вале кислотаи 100 %-и сулфат оҳанро нофаъол мекунад. Бо кислотаи нитрати консентратсияаш паст ва ё на он қадар баланд оҳан бо хориҷ намудани NO таъсири мутақобил мекунад:
Кислотаи консентронидаи нитрат оҳанро нофаъол мекунад.
d-Металлҳои гурӯҳи 11-уми системаи даврӣ. Ба
ин гурӯҳ мис, нуқра ва тилло дохил мешаванд. Конфигуратсияи ду қабати
охирини электронии ин элементҳо шакли умумии зеринро доранд:
ки дар ин ҷо n - рақами қабати
берунаи электронии элемент мебошад.
Ҳамаи элементҳои ин гурӯҳ металлҳои камфаъол буда, бо
мушкилӣ оксид мешаванд, бо об таъсири мутақобил намекунанд ва
ҳидроксидҳои онҳо асосҳои заиф мебошанд. Ин металлҳо дар қатори
электрохимиявии шиддат пас аз ҳидроген ҷойгир шудаанд. Онҳо якчанд
дараҷаи оксидшавиро зоҳир менамоянд. Мис дараҷаи оксидшавии +1 ва +2
зоҳир менамояд. Барои тилло дараҷаи оксидшавии +3 хос мебошад. Нуқра,
асосан, дараҷаи оксидшавии +1 дорад. Вале пайвастагиҳое низ маълуманд,
ки дар онҳо нуқра дараҷаи оксидшавии +2 ва +3 зоҳир менамояд.
Мис Cu. Мис аз назари химиявӣ
металли камфаъол мебошад.
Ҳангоми дар ҳаво гарм кардан вай то оксиди миси сиёҳ
(II) оксид мешавад:
Ҳангоми гарм кардан бо сулфур низ ба реаксия дохил мешавад:
Мис бо ҳалогенҳо дар ҳарорати мӯътадил таъсири мутақобил мекунад:
Кислотаҳои сулфат ва хлориди консентратсияашон паст ба мис таъсир намекунанд, вале дар иштироки оксиген ин кислотаҳо бо мис ба реаксия дохил мешаванд:
Мис бо
кислотаҳои консентронидаи нитрат ва сулфат низ ба реаксия дохил мешавад.
Нуқра Ag. Нуқра нисбат ба мис камфаъолтар аст.
Дар ҳаво на дар ҳарорати муқаррарӣ ва на ҳангоми гарм кардан оксид
намешавад.
Кислотаи хлорид ва кислотаи сулфати консентратсияашон
паст ба нуқра таъсир намекунанд. Нуқра дар кислотаи нитрат ҳал мешавад
ва бо он таъсири мутақобил мекунад:
Тилло Au. Тилло аз назари химиявӣ нисбат ба нуқра камфаъолтар аст. Онро ҳатто сахт гарм кунем ҳам, дар ҳаво тағйир намеёбад. Кислотаҳо ба тилло таъсир намекунанд. Тилло танҳо дар омехтаи муайяни кислотаҳои нитрат ва хлорид (шароби шоҳ) ҳал мешавад:
d-Металлҳои гурӯҳи 12-юми системаи даврӣ. Металлҳои ин гурӯҳ руҳ, кадмий ва симоб мебошанд. Конфигуратсияи ду қабати охирини электронии ин элементҳо шакли умумии зеринро дорад:
ки дар ин ҷо n - рақами қабати
берунаи электронии элемент аст.
Дар атомҳои руҳ, кадмий ва симоб
d-қишри қабати поёнтар аз қабати берунаи электронӣ пур шуда аст. Аз
ҳамин сабаб ин элементҳо дар пайвастагиҳои худ дараҷаи оксидшавии +2
зоҳир менамоянд.
Руҳ Zn. Руҳ
дар ҳаво бо пардаи оксидӣ пӯшида мешавад ва ин пардаи оксидӣ онро аз
оксидшавии минбаъда нигоҳ медорад.
Агар руҳро дар ҳаво сахт
гарм кунем, он гоҳ вай сӯхта, шӯълаи сафеди сабзтоб медиҳад ва оксиди
руҳ ҳосил мешавад:
Об ба руҳ қариб таъсир намекунад, зеро ки ҳидроксиди ҳосилшуда
дар об ҳалнашаванда аст ва он ба гузаштани реаксия монеъ мешавад.
Ҳалогенҳои беоб бо руҳ
таъсири мутақобил намекунанд, вале дар иштироки об онҳо бо руҳ ба
реаксия дохил шуда ҳалогенидҳо ҳосил менамоянд:
Омехтаи хокаи руҳ ва сулфур бо таркиш ба реаксия дохил мешаванд:
Руҳ бо кислотаҳои консентратсияашон паст ҳама вақт таъсири мутақобил мекунад:
Руҳ барқароркунандаи қавӣ мебошад. Вай бисёр металлҳои дувалентаро аз намакҳояшон берун карда метавонад:
Ҳангоми таъсири мутақобили руҳ бо кислотаи сероби нитрат, руҳ нитрогенро то нитрати аммоний барқарор мекунад:
Руҳ металли амфотерӣ аст ва бинобар ин вай дар ишқорҳо бо ҳосил намудани руҳатҳо (синкатҳо) ва ҳидроксоруҳатҳо ҳал мешавад:
Кадмий Cd. Бо хусусиятҳои асосиаш кадмий ба руҳ монанд аст,
вале бар хилофи руҳ кадмий хосияти амфотерӣ надорад.
Симоб Hg. Симоб
ягона металлест, ки дар ҳарорати муқаррарӣ моеъ мебошад. Вай дар байни
металлҳои ин гурӯҳ камфаъолтарин аст.
Симоб бо
кислотаҳои консентратсияашон паст ва ишқорҳо таъсири мутақобил намекунад.
Вай бо кислотаи
нитрат ва ҳангоми гарм кардан бо кислотаи консентронидаи сулфат ба
реаксия дохил мешавад:
Симоб бо оксиген дар ҳарорати бисёр баланд ба реаксия дохил мешавад:
Дар ҳамаи пайвастагиҳои симоб (I) атомҳои симоб бо ҳам пайвастанд ва аз ҳамин сабаб симоб дар ин пайвастагиҳояш дувалента мебошад:
Яке аз хусусиятҳои симоб аз он иборат аст, ки вай ҳаргиз ҳидроксидҳо ҳосил намекунад. Ҳатто ҳангоми таъсири ишқорҳо ба маҳлули намакҳои симоб (I) таҳшинии оксиди симоб (I) ҳосил мешавад: