|
|

|
| ||
|
|
||
► Боби I. Аминҳо. Аминокислотаҳо. Пайвастагиҳои ҳетеросиклии нитрогендор
► Амидҳо:сохт, истеҳсол ва хосиятҳои онҳо
► Аминокислотаҳо
► Намунаҳои ҳалли мисол ва масъалаҳо
► Мисол ва масъалаҳо барои ҳалли мустақилона
► Пайвастагиҳои ҳетеросиклии нитрогендор
► Савол ва супоришҳо ва таҷрибаҳои лабораторӣ
► Боби IV. Синтези моддаҳои калонмолекула ва масолеҳи полимерӣ дар асоси онҳо
► Методҳои асосии синтези полимерҳо
► Полимеризатсия
► Моддаҳои пластикӣ
► Каучукҳои синтезӣ
► Нахҳои синтезӣ
► Саволҳо ва таҷрибаҳои лабораторӣ ► Мисол ва масъалаҳо барои ҳалли мустақилона
► Боби V. Ҷамъбасти омӯзиши курси химияи органикӣ
► Намудҳои изомерия
► Изомерияи структурӣ
► Изомерияи занҷири атомҳои карбон
► Изомерияи ҳолати бандҳои дучанда ва сечанда дар молекула
► Изомерияи ҳолати гурӯҳҳои функсионалӣ ё атомҳои алоҳида дар молекула
► Изомерияе, ки ба пайвастагиҳои органикии дар таркиби молекулаашон ҳалқаи бензолӣ дошта хос аст
► Изомерияи фазоӣ ё стереоизомерия
► Табиати электронии банди химиявӣ
► Синтезҳои муҳими саноатӣ дар асоси коркарди нафт ва дигар ашёҳои карбоҳидрогенӣ
► Намунаи ҳалли масъалаҳо ва саволҳо барои ҷавоб
► Масъалаҳо барои ҳалли мустақилона
► Системаи даврии муосири элементҳои химиявӣ
► Мавқеи лантаноидҳо ва актиноидҳо дар системаи даврии элементҳои химиявӣ
► Валентнокӣ ва имкониятҳои валентии атомҳо
► Саволҳо барои ҷавоб ва намунаи ҳалли масъалаҳо
► Масъалаҳо барои ҳалли мустақилона
► Сохти фазоии молекулаи моддаҳои органикӣ ва ғайриорганикӣ
► Навъҳои панҷараҳои кристаллӣ ва хосияти моддаҳо
► Пайвастагиҳои комплексӣ
► Ададҳои координатсионӣ
► Системаҳои дисперсӣ
► Саволҳо барои ҷавоб ва намунаҳои ҳалли масъалаҳо
► Масъалаҳо барои ҳалли мустақилона
► Боби VIII. Реаксияҳои химиявӣ
► Таснифи реаксияҳои химиявӣ
► Суръати реаксияҳои химиявӣ
► Қонуни таъсири масса. Собити мувозинат
► Принсипи Ле-Шателе. Лағжиши мувозинати химиявӣ
► Катализ ва гидролиз
► Саволҳо барои ҷавоб ва намунаҳои ҳалли масъалаҳо
► Масъалаҳо барои ҳалли мустақилона
► Саҳми олимони асрҳои миёнаи тоҷик дар инкишофи химия
► Асосҳои илмӣ ва принсипҳои умумии технологияи химиявӣ
► Химия ва ҳифзи муҳити зист
► Химия дар ҳаёти мо
► Химиконии кишоварзӣ
► Саволҳо барои ҷавоб
► Замима
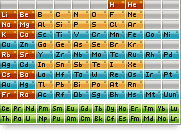

НАВЪҲОИ АСОСИИ БАНДИ ХИМИЯВИ
Шумо медонед, ки атомҳо моддаҳои содда ва мураккаб ҳосил мекунанд. Дар
ин моддаҳо атомҳо бо якдигар бо ёрии бандҳои гуногуни химиявӣ пайваст
мешаванд. Табиат ва хусусиятҳои банди химиявӣ аз сохти электронии
атомҳои пайвастшаванда вобаста аст. Яке аз мафҳумҳое, ки барои фаҳмидани
табиати банди химиявӣ ба мо кӯмак мерасонад, электроманфигии элементҳо
мебошад. Шумо бо ин мафҳум хуб шинос ҳастед. Электроманфигии элемент ин
нишондиҳандаи миқдории ба элемент ҷазб шудани электронҳо мебошад. Бо
сабаби хеле муҳим будани ин бузургӣ қимати он барои ҳамаи злементҳо дар
системаи даврӣ нишон дода шудааст. Аз системаи даврӣ аён аст, ки
электроманфигии элементҳо бо як низоми муайян тағйир меёбад. Дар даврҳо
электроманфигии элементҳо аз чап ба рост зиёд шуда, дар гурӯҳҳо аз боло
ба поён кам мешавад.
Бандҳои химиявӣ ба навъҳои зерин ҷудо карда мешаванд:
ионӣ, ковалентӣ (ғайриқутбӣ ва қутбӣ), металлӣ ва ҳидрогенӣ. Вале бояд
қайд кард, ки дар байни навъҳои банди химиявӣ сарҳади аниқе вуҷуд
надорад. Дар пайвастагиҳои химиявӣ бандҳои холис кам дучор шуда, бандҳое,
ки шакли омехта доранд, бештар вомехӯранд.
Банди ионӣ
Банди ионӣ дар натиҷаи пайваст шудани элементҳое, ки
электроманфигиашон аз якдигар фарқи бисёр калон доранд, ҳосил мешавад.
Дар ин маврид элементи электроманфигиаш хурд электронҳои қабати берунаи
электронии худро қариб пурра ба элементи электроманфигиаш калон дода, ба
иони зарядаш мусбат табдил меёбад. Дар навбати худ элементи
электроманфигиаш калон ин электронҳоро ба худ пайваст намуда ба иони
зарядаш манфӣ мубаддал мегардад. Дар байни ионҳои гуногунзаряд қувваи
кашиши кулонӣ амал мекунад, яъне банди химиявии ионӣ ҳосил мешавад. Ин
навъи банди химиявӣ махсусан ба пайвастагиҳое, ки металлҳои асил литий
Li, натрий Na, калий К, калсий Са, стронсий Sr, барий Ва бо
ғайриметаллҳо, масалан ҳалогенҳо, ҳосил мекунанд, хос аст.
Аммо бояд таъкид намуд, ки металлҳои ишқорӣ бо
элементҳои электроманфигиашон нисбатан калон, монанди оксиген ва сулфур,
ба маънои томи ин мафҳум банди ионӣ ҳосил намекунанд. Масалан, дар пай
вастагиҳои Li2O, Na2S бандҳои химиявӣ банди ионӣ
набуда, баръакс банди ковалентии қутбӣ мебошанд. Банди ионӣ, инчунин дар
ишқорҳо ва намакҳое, ки ба онҳо металлҳои фаъол ва оксиген дохил
мешаванд, дар байни атомҳои металлҳо ва оксиген ҳосил мешавад. Масалан,
дар ҳидроксиди натрий, NaOH ва сулфати натрий Na2SO4
танҳо банди байни натрий ва оксиген ионӣ мебошад. Аз ин сабаб маҳлули
обии ишқорҳо ва намакҳо чунин диссотсиатсия мешаванд:
Дар
байни ионҳо кашиши электростатикии зӯр мавҷуд аст, бинобар ин
пайвастагиҳои ионӣ ҳарорати баланди гудозиш доранд.
Банди ковалентӣ
Шумо аллакай бо ҳосилшавии банди ковалентӣ
шинос ҳастед ва медонед, ки он аз ҳисоби ҷуфти электронии умумӣ ҳосил
мешавад. Дар курси химияи органикӣ бо шаклҳои гуногуни бандҳои
ковалентие, ки дар натиҷаи пӯшидашавии абрҳои гуногуни электронӣ ҳосил
мешаванд, шинос шудед.
Акнун ба ин масъала вобаста бо
электроманфигии атомҳои ба ҳам пайвастшаванда дахл менамоем. Дар боло
дидем, ки агар электроманфигии атомҳои ба ҳам пайвастшаванда аз ҳамдигар
ба куллӣ фарқ кунанд, он гоҳ дар байни онҳо банди ионӣ ҳосил мешавад.
Агар электроманфигии атомҳои бо ҳам пайвастшаванда фарқ накунанд ва ё
фарқи хурд дошта бошанд, дар байни атомҳо чӣ гуна банди химиявӣ ҳосил
мешавад?
Банди ковалентии беқутб ё ғайриқутбӣ
Агар электроманфигии атомҳои бо ҳам
пайвастшаванда наздик бошад, банди химиявӣ дар байни атомҳо аз ҳисоби
ҷуфти электроние ҳосил мешавад, ки ҳар як атом онро аз электронҳои тоқи
қабати берунаи электрониаш медиҳад. Шумо аллакай медонед, ки ин гуна
банди химиявӣ банди ковалентӣ аст. Абрҳои электроние, ки ҷуфти умумии
электронӣ ҳосил мекунанд, нисбат ба ҳар ду атом ба таври симметрӣ ҷойгир
шудаанд ва аз ин сабаб марказҳои зарядҳои мусбат ва манфии атомҳо бо ҳам
мувофиқанд. Ин гуна бандҳои ковалентиро бандҳои ковалентии беқутб ё
ғайриқутбӣ меноманд. Чунин навъи бандҳо барои молекулаҳои дуатома,
аз қабили H2, F2, CI2, Вг2,
O2, N2, ва ғайра хос мебошад. Дар онҳо ҷуфти
электронӣ ба ҳар ду атом баробар тааллуқ дорад. Ҳамин тавр, ба хулосаи
зерин меоем:
Ҳангоми пайвастшавии атомҳои дорои электроманфигии якхела
дар байни атомҳо банди ковалентии беқутб ҳосил мешавад.
Банди ковалентии қутбнок (ё қутбӣ)
Дар ҳолати пайвастшавии атомҳое, ки
электроманфигиашон кам фарқ мекунанд, дар байни атомҳо аз ҳисоби ҷуфти
электронҳои умумӣ банди ковалентӣ ҳосил мешавад. Вале дар ин ҳолат,
бархилофи банди ковалентии беқутб, бо сабаби электроманфигии гуногун
доштани атомҳо, маркази абри электроние, ки ҷуфти умумии электронӣ ҳосил
мекунанд, ба тарафи атоми электроманфигиаш калонтар майл мекунад. Дар
натиҷа марказҳои зарядҳои мусбат ва манфии атомҳои бандро ҳосилкунанда
мувофиқ намеоянд. Аз ин сабаб банди ковалентии ҳосилшуда бо гаштовари (моменти)
диполии электрикӣ тавсиф карда мешавад. Ин гуна бандҳои ковалентиро
бандҳои ковалентии қутбнок ё қутбӣ меноманд. Чунин навъи бандҳо дар
молекулаи пайвастагиҳои ғайриорганикӣ, аз қабили HCl, H2O, H2S5NH3
ва ғайра дучор меоянд. Ҳамин тавр, ба хулосаи зерин меоем:
Ҳангоми пайваст шудани атомҳое, ки электроманфигиашон
фарқи кам доранд, дар байни атомҳо банди ковалентии қутбнок ҳосил меша
вад.
Ба бандҳои ковалентии қутбнок бандҳое, ки бо механизми донору
аксепторӣ ҳосил шудаанд, низ мансубанд. Мисоли ин гуна пайвастагиҳо
ионҳои ҳидроксоний ва аммоний шуда метавонанд. Дар пайвастагиҳои
органикӣ ва ғайриорганикӣ ин навъи банд паҳн шудатарин ба ҳисоб меравад.
Аз далелҳои дар боло овардашуда аён аст, ки дар механизмҳои
ҳосилшавии бандҳои ионӣ, ковалентии беқутб ва ковалентии қутбнок фарқи
асосӣ вуҷуд надорад. Онҳо танҳо бо дараҷаи қутбнокии абри электронии
молекулавӣ фарқ мекунанд. Банди ковалентии қутбнокро ҳамчун банде, ки
дар байни бандҳои ковалентии беқутб ва ионӣ меистанд, ҳисоб кардан
мумкин аст.
Банди металлӣ
Мо бо ду хели асосии банди химиявӣ, банди ионӣ ва
ковалентӣ шинос шудем. Акнун ба наъви дигари банди химиявӣ банди металлӣ
шинос мешавем.
Элементҳое, ки электроманфигии нисбатан кам доранд,
электронҳои қабати берунаи электронии худро ба осонӣ дода метавонанд. Аз
ин сабаб ҳангоми бо ҳам пайваст шудани чунин элементҳо, атомҳои ин
элементҳо дар зери таъсири майдони кулонии якдигар электронҳои қабати
берунаи электрониашонро гум карда, ба ионҳои мусбат табдил меёбанд.
Электронҳое, ки бо атомҳои алоҳида алоқамандиашонро гум кардаанд, барои
тамоми атомҳо умумӣ мегарданд ва дар байни ионҳо озод ҳаракат мекунанд.
Дар натиҷаи таъсири мутақобили ин электронҳои озод ва ионҳои мусбат
структураи муайяне арзи вуҷуд мекунад, ки дар он ионҳои мусбат панҷараи
фазоии муайянро ташкил менамоянд ва электронҳои умумишуда дар он
озододона ҳаракат мекунанд (расми 7). Дар ин ҳолат электронҳо ионҳои
мусбатро дар панҷараи металлӣ бо ҳам пайваст мекунанд.
Банди химиявие, ки дар натиҷаи кашиши электрикии
байни ионҳои мусбат ва электронҳои умумишуда ҳосил мешавад, банди
металлӣ ном дорад.
Аз гуфтаҳои боло бармеояд, ки банди металлӣ бо бандҳои
ионӣ ва ковалентӣ қаробат дорад. Монандиаш бо банди ковалентӣ дар он аст,
ки дар ҳар ду ҳолат электронҳои валентӣ умумӣ мегарданд. Аммо
фарқияташон дар он аст, ки агар дар банди ковалентӣ танҳо электронҳои
валентии ду атоми ҳамсоя умумӣ гарданд, ҳангоми ҳосилшавии банди металлӣ
ҳамаи электронҳои валентии атомҳо умумӣ мегарданд.
Умумияти банди металлӣ ва ионӣ дар он аст, ки дар ҳар ду ҳолат кашиши
байни элементҳои пайвастагӣ қувваи кашиши кулонӣ мебошад. Фарқи байни
банди металлӣ ва ионӣ аз он иборат аст, ки дар банди ионӣ кашиш дар
байни ионҳои гуногунзаряд, аммо дар банди металлӣ дар байни ионҳои
мусбат ва электронҳои озод ба вуҷуд меояд.
Аз сабаби он, ки дар металлҳо электронҳои озод бо
суръати хеле калон ҳаракат мекунанд ва барандаи зарядҳо мебошанд,
металлҳо гузаронандаи хуби ҷараёни электрикӣ мебошанд. Дар металлҳо
гармигузаронӣ низ тавассути электронҳо сурат мегирад. Аз ҳамин сабаб
металлҳо гармигузаронандаҳои хуб низ мебошанд.
Банди ҳидрогенӣ
Банди ҳидрогенӣ дар байни молекулаҳои моддаҳои гуногун,
ки дар таркибашон ҳидроген доранд, ҳосил мешавад. Вале барои ҳосил
шудани банди ҳидрогенӣ мавҷудияти атомҳои электроманфигиашон калон, аз
қабили F, O, N, Cl, S ва Вг, ки бо онҳо ҳидроген банди ковалентии
қутбнок ташкил мекунад, шарт ва зарур аст. Сабаби ба вуҷуд омадани банди
ҳидрогенӣ таъсири қувваҳои кулонӣ мебошанд.
Ҳангоми ҳосил шудани банди ковалентии қутбнок дар байни атоми
ҳидроген ва яке аз атомҳои дар боло овардашуда, масалан, атоми фтор F,
мо ин бандро чун диполи электрикие тасаввур карда метавонем, ки заряди
мусбаташ дар атоми ҳидроген, вале заряди манфиаш дар атоми фтор ҷой
гирифтааст. Бинобар ин дар байни атоми ҳидрогени як банди ковалентӣ ва
атоми фтори банди ковалентии дигар кашиши электростатикӣ (кулонӣ) ба
вуҷуд меояд, ки сабаби пайдошавии банди ҳидрогенӣ мегардад.
Дар моддаҳое, ки молекулаҳояшон аз ҳидроген ва атомҳои
электроманфигиашон калон (Р, О, N, Cl, S, Вг) иборат аст, дар байни
молекулаҳо банди ҳидрогенӣ мавҷуд аст. Дар об таъсири байниҳамдигарии
молекулаҳоро аз ҳисоби банди ҳидрогенӣ чунин ифода кардан мумкин аст:
Дар ин ҷо банди ҳидрогенӣ бо нуқтаҳо ишора карда шудааст.
Ба воситаи банди ҳидрогенӣ молекулаи моддаҳои дорои
банди ҳидрогенӣ, вобаста ба шароит, метавонанд гурӯҳҳои иборат аз ду (димер),
се (тример), n молекуларо ташкил кунанд, ки
онҳоро ассотсиатсияи молекулаҳо низ меноманд. Яъне, дар баъзе ҳолатҳо ин
молекулаҳо сохти полимерӣ доранд. Мо одат кардаем, ки таркиби обро бо
формулаи H2O ифода кунем, лекин
дурусттар мебуд, ки агар формулаи обро бо (H2O)n ифода кунем.
Дар ин ҷо n= 2,3, 4
ва ғайра буда метавонад.
Ҳамин тавр, дар моддаҳои дигаре, ки банди ҳидрогенӣ доранд,
чун аммиак, ҳидрогенфторид, спиртҳо, кислотаҳои органикӣ ва ғайра
ҳамчунин ассотсиатсияи молекулаҳо ба вуҷуд
меояд. Маҳз аз ҳамин сабаб ҳарорати гудозиш ва ҷӯшиши
спиртҳо нисбат ба карбоҳидрогенҳои мувофиқашон баландтар аст.
Бояд қайд
намоем, ки дар қатори HF, H2O, NH3, HCI, H2S
энергияи банди ҳидрогенӣ кам мешавад. Бо баланд шудани ҳарорат низ
энергияи банди ҳидрогенӣ кам мешавад. Банди ҳидрогенӣ нисбат ба бандҳои
ионӣ ва ковалентӣ заифтар мебошад.
Банди ҳидрогенӣ барои бисёр пайвастагиҳои органикӣ (фенолҳо,
алдегидҳо, кислотаҳои карбон ва ғ.) хос
мебошад. Аз ҳисоби бандҳои ҳидрогенӣ структураи дуюмини сафедаҳо,
спирали дучандаи КДН ҳосил мешавад.