|
|

|
| ||
|
|
||
► Боби I. Аминҳо. Аминокислотаҳо. Пайвастагиҳои ҳетеросиклии нитрогендор
► Амидҳо:сохт, истеҳсол ва хосиятҳои онҳо
► Аминокислотаҳо
► Намунаҳои ҳалли мисол ва масъалаҳо
► Мисол ва масъалаҳо барои ҳалли мустақилона
► Пайвастагиҳои ҳетеросиклии нитрогендор
► Савол ва супоришҳо ва таҷрибаҳои лабораторӣ
► Боби IV. Синтези моддаҳои калонмолекула ва масолеҳи полимерӣ дар асоси онҳо
► Методҳои асосии синтези полимерҳо
► Полимеризатсия
► Моддаҳои пластикӣ
► Каучукҳои синтезӣ
► Нахҳои синтезӣ
► Саволҳо ва таҷрибаҳои лабораторӣ ► Мисол ва масъалаҳо барои ҳалли мустақилона
► Боби V. Ҷамъбасти омӯзиши курси химияи органикӣ
► Намудҳои изомерия
► Изомерияи структурӣ
► Изомерияи занҷири атомҳои карбон
► Изомерияи ҳолати бандҳои дучанда ва сечанда дар молекула
► Изомерияи ҳолати гурӯҳҳои функсионалӣ ё атомҳои алоҳида дар молекула
► Изомерияе, ки ба пайвастагиҳои органикии дар таркиби молекулаашон ҳалқаи бензолӣ дошта хос аст
► Изомерияи фазоӣ ё стереоизомерия
► Табиати электронии банди химиявӣ
► Синтезҳои муҳими саноатӣ дар асоси коркарди нафт ва дигар ашёҳои карбоҳидрогенӣ
► Намунаи ҳалли масъалаҳо ва саволҳо барои ҷавоб
► Масъалаҳо барои ҳалли мустақилона
► Системаи даврии муосири элементҳои химиявӣ
► Мавқеи лантаноидҳо ва актиноидҳо дар системаи даврии элементҳои химиявӣ
► Валентнокӣ ва имкониятҳои валентии атомҳо
► Саволҳо барои ҷавоб ва намунаи ҳалли масъалаҳо
► Масъалаҳо барои ҳалли мустақилона
► Сохти фазоии молекулаи моддаҳои органикӣ ва ғайриорганикӣ
► Навъҳои панҷараҳои кристаллӣ ва хосияти моддаҳо
► Пайвастагиҳои комплексӣ
► Ададҳои координатсионӣ
► Системаҳои дисперсӣ
► Саволҳо барои ҷавоб ва намунаҳои ҳалли масъалаҳо
► Масъалаҳо барои ҳалли мустақилона
► Боби VIII. Реаксияҳои химиявӣ
► Таснифи реаксияҳои химиявӣ
► Суръати реаксияҳои химиявӣ
► Қонуни таъсири масса. Собити мувозинат
► Принсипи Ле-Шателе. Лағжиши мувозинати химиявӣ
► Катализ ва гидролиз
► Саволҳо барои ҷавоб ва намунаҳои ҳалли масъалаҳо
► Масъалаҳо барои ҳалли мустақилона
► Саҳми олимони асрҳои миёнаи тоҷик дар инкишофи химия
► Асосҳои илмӣ ва принсипҳои умумии технологияи химиявӣ
► Химия ва ҳифзи муҳити зист
► Химия дар ҳаёти мо
► Химиконии кишоварзӣ
► Саволҳо барои ҷавоб
► Замима
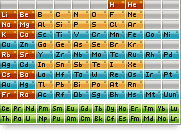

Ба саволҳо ҷавоб диҳед
1. Сохти атом ва моддаҳои соддаи
ғайриметаллҳо ва металлҳо бо чӣ фарқ мекунанд?
2. Дар асоси системаи даврӣ қонуниятҳоеро, ки тағйирёбии хосиятҳои
оксиду барқароршавии ғайриметаллҳоро муайян мекунанд, шарҳ диҳед.
3. Хосиятҳои химиявии ғайриметаллҳои муҳим ва истифодабарии онҳоро баён
кунед.
4. Дар тағйирёбии хосиятҳои оксидҳои кислотагӣ дар даврҳо ва гурӯҳҳо
кадом қонуният мушоҳида мешавад?
5. Формулаи оксидҳои кислотагии зерин дода шудаанд: a) N2O5,
CO2, Cl2О7 ва SO3; б) P2O5,
As2O5, N2О5 ва Sb2O5.
Онҳоро бо тартиби афзудани хосиятҳои кислотагиашон ҷойгир намоед.
6. Хосиятҳои фарқкунанда ва монандии кислотаҳои нитрат ва сулфатро нишон
диҳед.
7. Дар вақти таъсири мутақобили кислотаи консентронидаи сулфат бо оҳан
дараҷаи оксидшавии сулфур аз +6 то +4 тағйир меёбад. Муодилаи мувофиқро
тартиб диҳед.
8. Барои чӣ пайвастагиҳои ҳидрогении бухорнашаванда аз пайвастагиҳои
ҳидрогении бухоршаванда фарқи калон доранд?
9. Муодилаи реаксияҳоеро тартиб диҳед, ки бо ёрии онҳо табаддулоти зерин
иҷро шавад:
Муодилаҳоро бо тарзи кӯтоҳ ва пурраи ионӣ тасвир кунед.
Ҳал:
Намунаи ҳалли масъалаҳо
1) Чанд ҳаҷм обро бо чанд ҳаҷм маҳлули 96%-и H2SO4 (р=1,84г/см3) илова намоем, ки маҳлули 15% H2SO4(P=1,1 г/см3) ҳосил шавад?
Ҳал.
Ҳаҷми маҳлули 96%-и H2SO4-ро
бо X ишора мекунем. Он гоҳ массаи он ба mM1=p1·X
баробар аст.
Аз таърифи ҳиссаи массавӣ
массаи кислотаи сулфатро дар маҳлули аввала меёбем:
Ҳаҷми оби ба маҳлули аввала ҳамроҳ кардашударо бо У ишора мекунем. Он гоҳ ҳаҷми маҳлули дуюм ба X + У баробар мешавад. Массаи ин маҳлул ба
баробар аст.
Аз таърифи ҳиссаи массавӣ
формулаҳои зерин бармеоянд:
Муодилаҳои (4) и (6)-ро баробар карда, ба он массаи кислотаи сулфатро мегузорем. Он гоҳ аз муодилаи (2) ҳосил мекунем:
Қиматҳои ададӣ гузошта, ба муодилаи зерин меоем:
Яъне, агар ба ҳар як ҳаҷм маҳлули 96%-а
9,7 ҳаҷм об илова намоем, маҳлу ли 15%-а ҳосил
мешавад.
Ҷавоб: (як
ҳаҷм кислота, 9,7 ҳаҷм об)
2) Аз маҳлуле, ки дар
100 мл об 2 г омехтаи хлориди натрий ва йодиди
натрий дорад, 1 л хлори газмонандро гузарониданд. Маҳлули ҳосилшударо буғронӣ
намуда, таҳшиниро дар ҳарорати 200-300°С
тафсониданд. Дар натиҷа 1,78 г таҳшинӣ боқӣ монд. Массаи намакҳо дар
омехтаи аввала ёфта шавад.
Ҳал.
Чӣ хеле ки ба мо маълум аст,
хлориди натрий бо хлор ба реаксия намеравад. Пас, массаи омехта аз
ҳисоби хориҷшавии йод 2-1,78=0,22 г кам
мешавад. Агар массаи хлорро бо X ишорат кунем, пас, массаи йоди
хориҷшуда аз массаи хлор 0,22 г зиёда аст, яъне mj2
= X + 0,22 . Ин ифодаро ба муодилаи реаксия гузошта, муодилаи зеринро
тартиб медиҳем:
Массаи йодиди натрии
ба реаксия дохилшавандаро ба воситаи массаи
хлори ба реаксия дохилшуда
ва массаи оби ҳосилшуда
ифода карда метавонем. Ин ду ифодаро баробар намуда ҳосил мекунем:
Аз рӯи массаи хлори ба реаксия дохилшуда массаи йодиди натрийро меёбем:
Ҷавоб: 0,36 г NaI, 1,64 г NaCl.
3) Дар 100 г маҳлули 91%-и
кислотаи сулфат чанд грамм SO3-ро
ҳал намоем, ки олеуми 30%-а ҳосил шавад?
Ҳал.
Массаи SO3-и
зарурӣ аз ду қисм иборат аст: қисми аввал массаи SO3-е
мебошад, ки бояд бо оби боқимонда дар маҳлули 91%-аи
H2SO4 таъсири мутақобил намояд ва қисми дуюм
массаи SO3 мебошад, ки барои ҳосил намудани олеуми 30%-а
зарур аст.
Барои муайян намудани қисми
аввали SO3, дар аввал, миқдори оби дар 100г маҳлули 91%-и
кислотаи сулфат мавҷудбударо меёбем ва сипас, миқдори кислотаи сулфатеро,
ки ҳангоми ҳалшавии қисми аввали SO3 дар маҳлули 91%-и
H2SO4 ҳосил мешавад, муайян мекунем.
Азбаски ҳиссаи массавии H2SO4
дар маҳлул ба 91% баробар аст, он гоҳ ҳиссаи массавии об ба 9% баробар
мешавад. Массаи об ва H2SO4-ро
меёбем:
Муодилаи реаксияро навишта ҳосил мекунем:
Массаи умумии кислотаи сулфат, ки барои ҳосил намудани олеум ҳамчун ҳалкунанда хизмат мекунад, ба суммаи массаҳои кислотаи сулфати ҳосилшуда ва кислотаи сулфати дар маҳлул буда баробар аст:
Микдори SO3-и барои ҳосил намудани олеуми 30%-а зарурро аз таносуби зерин меёбем:
Ҷавоб: 100 г SO3